西新井江北クリニックドクターより
こんにちは(メリークリスマス)。
西新井江北クリニックの医師 前田です。
今週は私がブログ記事の担当ということで、いくつか論文を紹介したいと思います。
ご存知の通り、新型コロナウイルス(SARS-CoV-2)の第3波が襲来しています。
SARS-CoV-2は世界的な規模での問題なので、研究結果が数多く出ており、また、早急に沈静化を図るべく、本来ならば有料の最新論文が、無料で読める学術雑誌が多くなっています。
折角の機会ですので、記事内にリンクを貼っていますので、是非、目を通してみられることをお勧めします(もちろん英語です)。
SARS-CoV-2について、最近もいくつか重要な論文が出ています。
その1つが、Science誌に発表された、SARS-CoV-2が宿主の細胞に感染する際に必要な新しいターゲットが発見されたという研究結果です(https://science.sciencemag.org/content/370/6518/856/tab-pdf、https://science.sciencemag.org/content/370/6518/861/tab-pdf)。
そして、NEJM誌には、SARS-CoV-2のRNAワクチン(ファイザー製ワクチン)の効果に関する研究結果が発表されています(https://www.nejm.org/doi/pdf/10.1056/NEJMoa2034577?articleTools=true)。
ワクチンは、ウイルスの感染メカニズムと切っても切り離せないため、1つ目の話題に関連して紹介したいと思います。
なお、「病原体とは」、「ウイルスとは」、「コロナウイルスとは」などといった概念は、予備知識として必要なのですが、そこまでは紹介できないので、各自で勉強して頂ければと思います。
なお、SARS-CoV-2の侵入、感染の流れ(および創薬ターゲット)は、下記の図などが分かりやすいと思いますので、参考にして下さい。
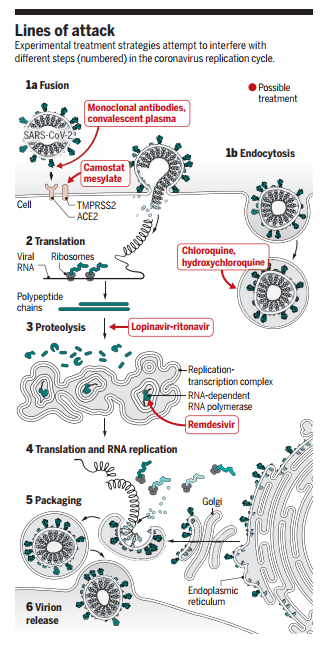
図1:https://science.sciencemag.org/content/367/6485/1412/tab-pdf
また、ブログ記事という都合上、大まかな説明になる(加えて、研究の世界における論文紹介のルールからは逸脱する)ことをご容赦下さい。
まず1つ目の話題です。
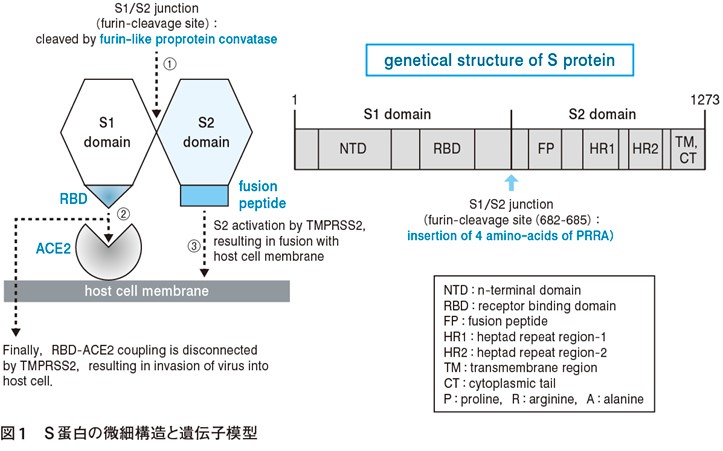
図2:https://www.jmedj.co.jp/journal/paper/detail.php?id=15298
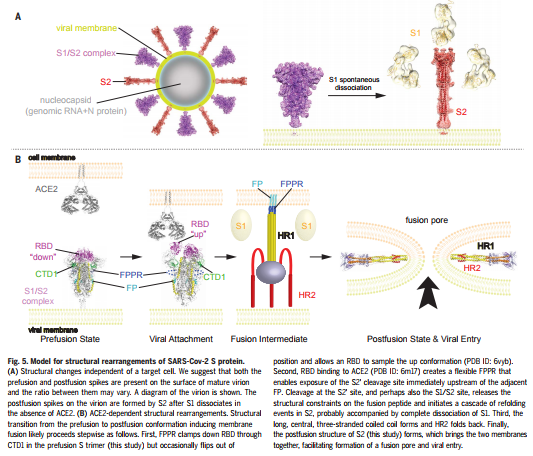
図3:https://science.sciencemag.org/content/369/6511/1586/tab-pdf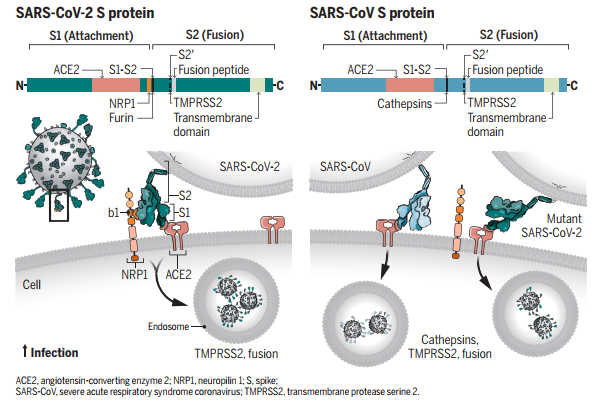
図4:https://science.sciencemag.org/content/370/6518/765/tab-pdf
SARS-CoV-2が宿主の細胞に感染する際、
①SARS-CoV-2のSpike蛋白(S1+S2)が、宿主の細胞表面にあるproteaseによって、S1とS2に分離
②SARS-CoV-2のSpike蛋白 S1にあるreceptor binding domain(RBD)が、宿主の細胞表面のACE2受容体に結合
③SARS-CoV-2のSpike蛋白 S2が、宿主の細胞表面のtransmembrane protease serine2(TMPRSS2)によって活性化
④活性化したSARS-CoV-2のSpike蛋白 S2が、そのfusion peptideを介して、宿主の細胞膜に融合
⑤SARS-CoV-2のSpike蛋白 S1にあるreceptor binding domain(RBD)と宿主の細胞表面のACE2受容体が、宿主の細胞表面のtransmembrane protease serine2(TMPRSS2)によって切断
その結果、SARS-CoV-2が宿主の細胞内に侵入、感染します(図2を参照、実際はもっと複雑な形態変化の過程があり、それは図3を参照)。
①の「宿主の細胞表面にあるprotease」について、2002から2003年に流行した、いわゆるSRASウイルス(SARS-CoV)はcathepsins、SARS-CoV-2はfurinを用いていることまでは分かっていました。
しかし、SARS-CoVとSARS-CoV-2の感染性の違いを説明することはできていませんでした。
今回、前者の論文の著者らは、in vitroの系において、
(1)まず、SARS-CoV-2のSpike蛋白 S1と宿主の細胞表面のNeuropilin-1(NRP1)が相互作用して、SARS-CoV-2の感染を増強すること
(2)次に、X線結晶構造解析という方法を用いることで、SARS-CoV-2のSpike蛋白 S1のfurinによって切断された配列が、宿主の細胞表面のNeuropilin-1(NRP1)に直接結合し得ること
(3)最後に、SARS-CoV-2のSpike蛋白 S1と宿主の細胞表面のNeuropilin-1(NRP1)の結合を阻害することで、SARS-CoV-2の感染を減弱すること
を示しました。
また、後者の論文の筆者らは、これも基本的にはin vitroの系において、
(1)まず、宿主の細胞表面のNeuropilin-1(NRP1)が、SARS-CoV-2の宿主細胞への侵入を促進すること
(2)次に、宿主の細胞表面のNeuropilin-1(NRP1)を抗体によりブロックすると、遺伝子改変をしていないSARS-CoV-2は感染が減弱するのに対し、furinによって分離される配列を遺伝子改変したSARS-CoV-2では感染が減弱しないこと
(3)また、宿主の細胞表面のNeuropilin-1(NRP1)が、SARS-CoV-2のSpike蛋白 S1のfurinによって切断された配列と同じ配列を持つナノ粒子の、培養細胞、嗅覚上皮細胞、マウスの中枢神経細胞への侵入を仲介すること
(4)最後に、covid-19の患者の、SARS-CoV-2が感染している嗅覚上皮細胞において、宿主の細胞表面のNeuropilin-1(NRP1)が高発現していることを
を示しました。
この2つの結果から、宿主の細胞表面のNeuropilin-1(NRP1)が、SARS-CoV-2の侵入、感染において、重要な役割を担っていることが、予備的ではありますが示されました。
つまりは、SARS-CoV-2が、宿主の細胞表面にあるproteaseであるtransmembrane protease serine2(TMPRSS2)だけでなく、Neuropilin-1(NRP1)も用いることで、SARS-CoVに比べ、侵入、感染しやすくしていると考えられます(図4)。
Neuropilin-1(NRP1)という、SARS-CoVとSARS-CoV-2の感染性の違いをリーズナブルに説明するターゲットが発見されたことは、SARS-CoV-2に対する創薬において、かなり大きな進歩であると考えられ、SARS-CoV-2の感染制御への期待がかかるところです。
余談になりますが、SARS-CoV-2のSpike蛋白 S1にあるreceptor binding domain(RBD)に関する研究はさかんにされており、今回の論文の後に、Science誌だけでも3本の論文が出てます。
これらの論文を始め、SARS-CoV-2に関する色々な論文において、SARS-CoV-2の流行前から、私個人的に熱かったX線結晶構造解析が使われており、嬉しいところです。
さて、こちらはさっと行きたいのですが、2つ目の話題です。
世界中でSARS-CoV-2のワクチン競争が繰り広げられており、臨床試験のデータが出てきていますし、一般に向けたワクチン接種が始まっている国があります。
おそらく日本でも、今回の論文に出てくる、ファイザー社製のRNAワクチン(BNT162B2)が最初に接種されると予想されます。
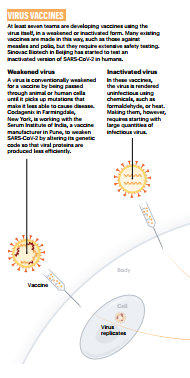
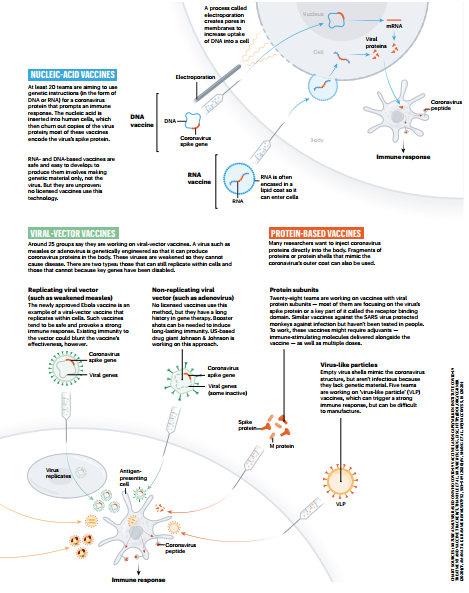
図5:https://media.nature.com/original/magazine-assets/d41586-020-01221-y/d41586-020-01221-y.pdf
ワクチンとは、詳細は控えますが、例えばSARS-CoV-2の場合、SARS-CoV-2の一部を体内の免疫細胞に認識させることで、SARS-CoV-2に対する免疫誘導をする(いわゆる免疫をつける)方法です。
では、何を体内の免疫細胞に認識させるかというと、基本的に、1つ目の話題で出てきた、SARS-CoV-2のSpike蛋白、特にSpike蛋白 S1にあるreceptor binding domain(RBD)をターゲットとしています。
また、SARS-CoV-2の一部を体内の免疫細胞に認識させる方法は色々ありますが、今回の論文のワクチンは、ターゲットと同じmessenger RNA(mRNA)を脂質の膜に包んで粒子状にしたものを、注射で投与する方法です。
その結果、SARS-CoV-2のSpike蛋白 S1にあるreceptor binding domain(RBD)と同じ蛋白が体内で作られ、それを免疫細胞が認識することで、SARS-CoV-2に対する免疫誘導がされます。
インフルエンザワクチンなど、今までの他のウイルスに対するワクチンは、基本的に、ウイルス自体を弱くした、もしくは、不活化したもので、今回のRNAウイルスとはまったく異なります。
RNAワクチンが認可されれば、初めてのRNAワクチンとなるわけですが、まだ分からないことがたくさんあり、今後の推移を見守る必要があります(https://news.yahoo.co.jp/byline/kimuramasato/20201120-00208764/、日本語の記事で、少し論点が違う部分もありますが、役に立つと思います)。
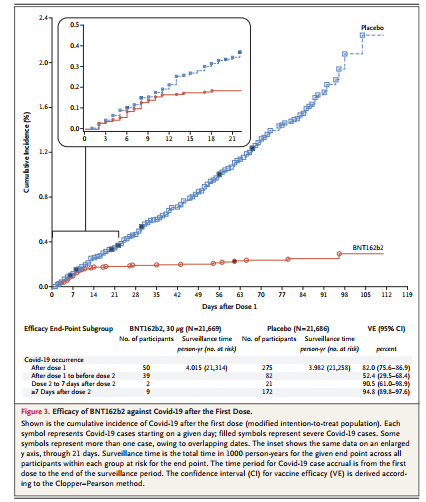
図6:https://www.nejm.org/doi/pdf/10.1056/NEJMoa2034577?articleTools=true
さて、今回の論文に出てくる、ファイザー社製のRNAワクチン(BNT162B2)の効果ですが、ワクチンを接種した群では、接種していない群に比べて、SARS-CoV-2の発症を95%抑制したという結果で、はっりとした有効性が示されました。
また、ワクチン接種による有害事象は、重篤なものはなく、有害事象自体もワクチンを接種した群と接種していない群で有意な差はなかったという結果でした。
なお、95%の抑制効果というのは、単純には比較できないものの、インフルエンザワクチンと比べても、かなりいい数値になります。
ただし、感染ではなく発症の抑制であり、どのぐらいの流行抑制ができるのか、長期間、年齢別での効果はどのぐらいあるのかなど、効果についてだけでも、今後の推移を見守るべき点はたくさんあるかと思います。
今回の論文の後、臨床試験の細かい解析結果についての論文も出てきており、今後の進展が期待されます。
最後に、上記以外のSARS-CoV-2に関する興味深い論文を挙げておきます(感染期間について)。
・https://www.nature.com/articles/s41591-020-0869-5
・https://www.thelancet.com/action/showPdf?pii=S2666-5247%2820%2930172-5
こういったSARS-CoV-2の特徴が、1つ目の話題レベルで語れるようになると面白いなと思います。
もう残すところ、今年も1週間。
この1年、西新井江北クリニックで、主として診療をさせて頂き患者さんから色々なことを学びました。
長くなりましたが、今年もお世話になりました。
来年も宜しくお願い致します。
よいお年を。
そして、来年はいい年になりますように。
前田








